2021年2月22日,东南大学生命科学与技术学院柴人杰教授课题组李异媛副研究员联合浙江大学靳津教授实验室在Journal of Experimental Medicine (JEM)发表题为" Single-nucleotide methylation specifically represses type I interferon in antiviral innate immunity"的研究论文,揭示了DNA甲基化在调节抗病毒先天免疫中的重要作用和分子机制。
随着H1N1、脊髓灰质炎、埃博拉、寨卡和COVID-19的爆发,病毒引起的感染越来越受到人们关注。另外,季节性流感在世界范围内引起严重的发病率和死亡率,并造成巨大的经济损失。因此,阐明抗病毒感染的分子机制十分重要。
近年来,研究发现DNA甲基化参与干扰素的调控。斑马鱼中Uhrf1或者Dnmt1的突变,导致I类反转录转座子的诱导表达和细胞质DNA病毒感受器激活,进而通过Sting信号通路促使干扰素表达增加。TET3通过招募组蛋白去乙酰化酶1(HDAC1)和转录共抑制因子(SIN3A)到Ifnb1的启动子区,抑制I型IFN的转录,这个过程不依赖于DNA去甲基化。另外,DNA甲基化抑制剂5-氮胞苷(5-azacytidine,AZA)通过DNA去甲基化上调内源性逆转录病毒的转录,进而通过RNA感受器介导的信号通路促进干扰素IFN-b的分泌。但是与AZA处理导致的去甲基化不同,内源性去甲基化肿瘤中内源性逆转录病毒表达与免疫活性标志物的表达并不是正相关,而是负相关,这说明IFN-a/b信号的失活擦除了由于基因组去甲基化引起的内源性逆转录病毒表达的免疫刺激作用。因此探索表观遗传疗法的不同作用机制具有重要的潜在价值。
该研究发现,髓系细胞中Uhrf1的缺失可显著上调Ifnb的表达,增强对病毒感染的抵抗能力。通过全基因组亚硫酸氢盐测序(WGBS),该课题组发现Ifnb启动子区域的一个单核苷酸甲基化位点干扰了IRF3的招募。随后该课题组使用该位点特异性突变敲入小鼠和区域特异性去甲基化工具确认了该甲基化位点在调节Ifnb表达和抗病毒反应中起关键作用。这些发现为DNA甲基化在先天性抗病毒免疫反应中的调控提供了重要信息。
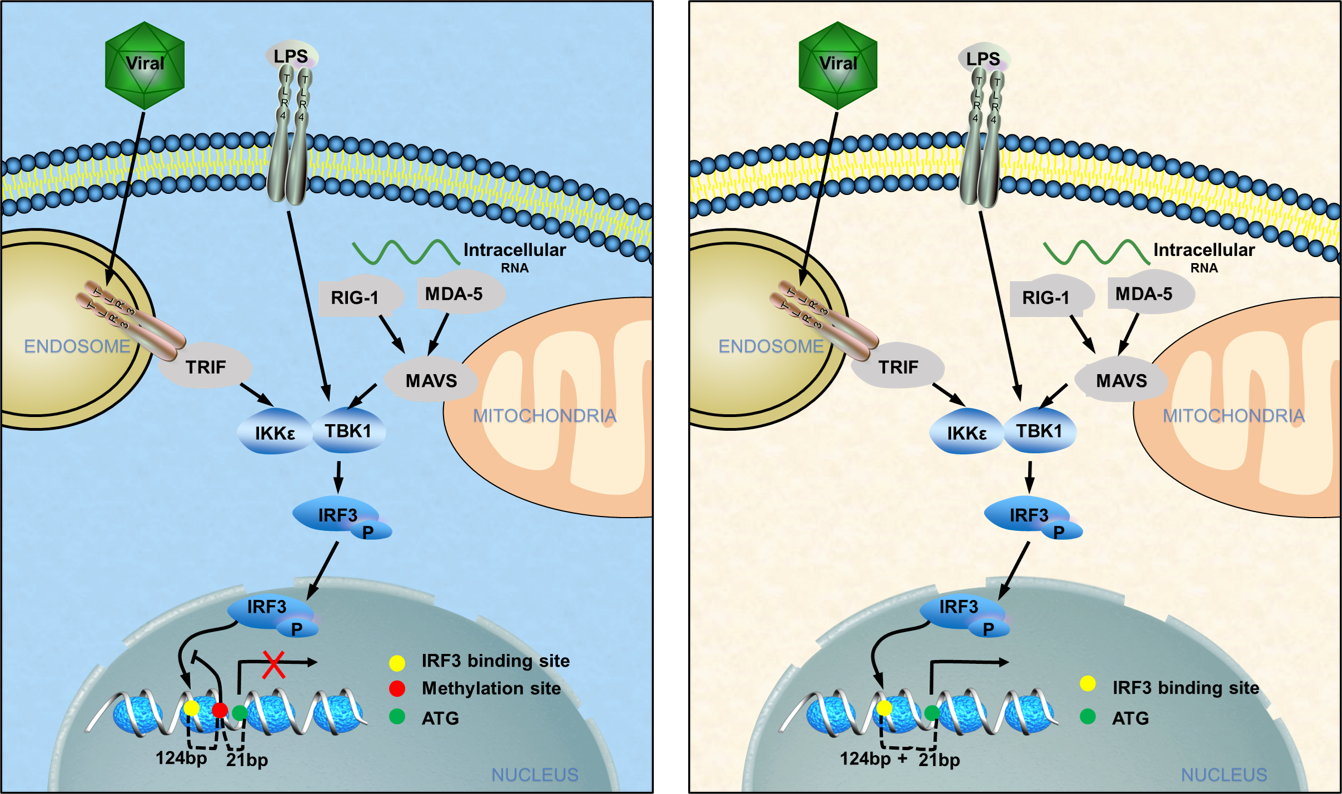
该工作揭示了调控IFN-I诱导表达的独特机制,并通过靶向抗病毒先天免疫中的DNA甲基化建立了一个重要的治疗工具。
本课题高正君博士和博士研究生李文平为共同一作,李异媛副研究员和靳津教授为本文的共同通讯作者。该项研究获得了国家重点研发项目,中国优秀青年科学家基金,浙江省自然科学基金,中国国家自然科学基金和浙江省的关键研究和发展项目的资助。
原文链接:https://rupress.org/jem/article-abstract/218/3/e20201798/211817/Single-nucleotide-methylation-specifically?redirectedFrom=fulltext



